Nueva nomenclatura internacional de dispositivos médicos impulsada por la OMS
Fecha: Febrero 2019
Idioma: Castellano
Procedencia: Meirovich Consulting
Web: ver aquí
Autor: Rocío Pestaña Martínez, Claudio Meirovich
Las nomenclaturas de los dispositivos médicos son sistemas diseñado para identificar en mayor o menor medida todos los dispositivos considerados “médicos” así como productos de salud relacionados, asignando a cada uno de ellos un nombre genérico. El uso de una nomenclatura permite estandarizar términos, lo que facilita su regulación y asegura una mejor comunicación y comercialización de dichos productos lo que permitiría entre otras cosas romper las barreras lingüísticas que hoy existen a nivel mundial [1].
Situación actual en el uso de nomenclaturas para dispositivos médicos
Diversos países han desarrollado su propio sistema de nomenclatura nacional, sin embargo, los más utilizados son la nomenclatura global de los productos sanitarios (GMDN) y la nomenclatura universal de equipos médicos (UMDNS).
Estos sistemas se utilizan para intercambiar datos e información de los distintos productos entre farmacéuticos, reguladores y autoridades sanitarias, respaldar el control del inventario dentro de los hospitales, así como, para facilitar la compra y gestión de los distintos suministros.
El código GMDN consiste en un código único para cada producto formado por cinco dígitos asociados a un término, una definición y la categoría de cada dispositivo en concreto. UMDNS también usa un código de cinco dígitos, pero los asigna en consecutiva sin que tengan un significado intrínseco.
Este número (casi podría decirse aleatorio) es único y está asociado a una definición y descripción del uso del dispositivo [1]. En 2010 el departamento de tecnologías sanitarias esenciales perteneciente a la Organización Mundial de la Salud (OMS) lanzó una encuesta de referencia por países con el fin de determinar de qué manera era necesario apoyar a los diferentes países en el desarrollo de programas para la gestión e impulso de tecnologías sanitarias.
Este estudio detectó que el 52% de los países participantes en el estudio utilizan por lo menos uno de los denominados sistemas de nomenclatura “oficiales” existentes; que el 26% de los países ha desarrollado un sistema nacional; que el 12% utiliza UMDNS; el 10% GMDN y el 3% usan más de uno.
Sin embargo, el dato alarmante es que el 48% de los países restantes no cuentan con ningún sistema nacional de nomenclatura para dispositivos médicos [2]. Las nomenclaturas de los dispositivos médicos son sistemas diseñado para identificar en mayor o menor medida todos los dispositivos considerados “médicos” así como productos de salud relacionados, asignando a cada uno de ellos un nombre genérico.
El uso de una nomenclatura permite estandarizar términos, lo que facilita su regulación y asegura una mejor comunicación y comercialización de dichos productos lo que permitiría entre otras cosas romper las barreras lingüísticas que hoy existen a nivel mundial [1].
Situación actual en el uso de nomenclaturas para dispositivos médicos
Diversos países han desarrollado su propio sistema de nomenclatura nacional, sin embargo, los más utilizados son la nomenclatura global de los productos sanitarios (GMDN) y la nomenclatura universal de equipos médicos (UMDNS).
Estos sistemas se utilizan para intercambiar datos e información de los distintos productos entre farmacéuticos, reguladores y autoridades sanitarias, respaldar el control del inventario dentro de los hospitales, así como, para facilitar la compra y gestión de los distintos suministros.
El código GMDN consiste en un código único para cada producto formado por cinco dígitos asociados a un término, una definición y la categoría de cada dispositivo en concreto. UMDNS también usa un código de cinco dígitos, pero los asigna en consecutiva sin que tengan un significado intrínseco.
Este número (casi podría decirse aleatorio) es único y está asociado a una definición y descripción del uso del dispositivo [1]. En 2010 el departamento de tecnologías sanitarias esenciales perteneciente a la Organización Mundial de la Salud (OMS) lanzó una encuesta de referencia por países con el fin de determinar de qué manera era necesario apoyar a los diferentes países en el desarrollo de programas para la gestión e impulso de tecnologías sanitarias.
Este estudio detectó que el 52% de los países participantes en el estudio utilizan por lo menos uno de los denominados sistemas de nomenclatura “oficiales” existentes; que el 26% de los países ha desarrollado un sistema nacional; que el 12% utiliza UMDNS; el 10% GMDN y el 3% usan más de uno.
Sin embargo, el dato alarmante es que el 48% de los países restantes no cuentan con ningún sistema nacional de nomenclatura para dispositivos médicos [2]. [caption id="attachment_333539" align="aligncenter" width="883"]
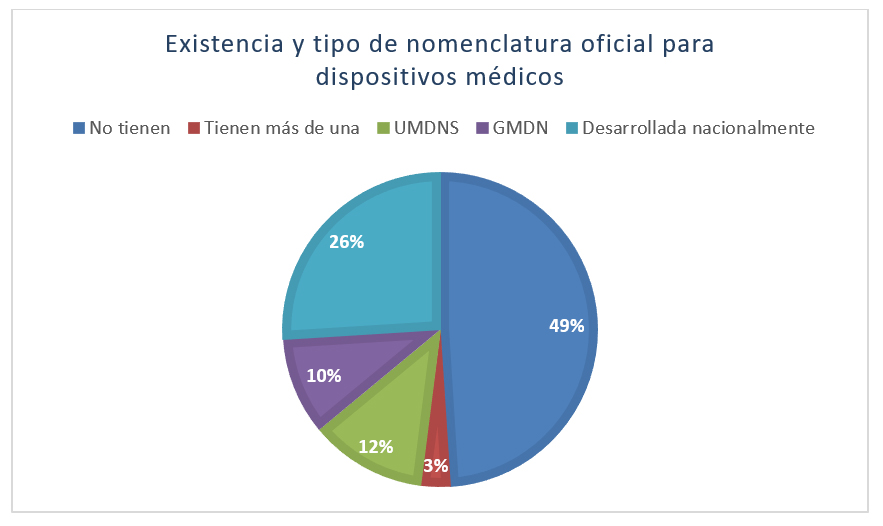 Ilustración 1: Existencia y tipo de nomenclatura oficial para dispositivos médicos[/caption]
Ilustración 1: Existencia y tipo de nomenclatura oficial para dispositivos médicos[/caption]
El amplio número de sistemas utilizados en todo el mundo y la distribución tan dispar de estos códigos claramente dificultan la comunicación entre las distintas organizaciones y empresas que trabajan en este sector.
En este contexto, la OMS decidió crear un sistema de nomenclatura de dispositivos médicos unificado que pueda ser utilizado globalmente por todo el mundo con el fin de mejorar el acceso, la calidad y el uso de productos médicos y tecnologías sanitarias [3]. La creación de este “sistema de nombrado” común puede traer consigo diversos beneficios incluyendo el incremento de la seguridad del paciente al poder garantizar una mayor vigilancia y trazabilidad de los productos comercializados [3]. Actualmente, por ejemplo, el estudio o análisis de los efectos adversos relacionados con un determinado producto están muy limitados debido a la escasa información específica o técnica que se tiene sobre él. Otras de las ventajas que se espera conseguir con una nomenclatura única es acelerar los procesos regulatorios, facilitar la selección de los distintos productos o ayudar en la compra y administración de los dispositivos, así como mejorar la comunicación entre las distintas entidades relacionadas con los dispositivos médicos.
Para poder escribir un comentario debe iniciar sesión o darse de alta en el portal.